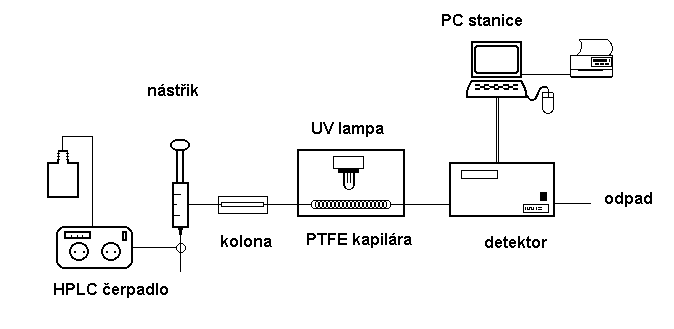
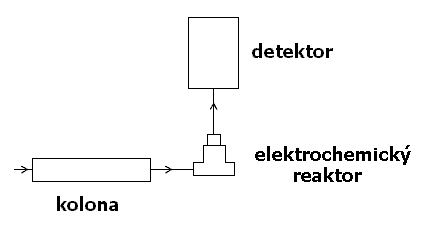
Postkolonová derivatizace v HPLC (Post-column derivatization)
1. Požadavky na deriváty postkolonové derivatizace
- derivatizační reakce nemusí poskytovat jednoznačné chemické individuum
- derivatizační reakce nemusí probíhat kvantitativně, ale rozhodující je dobrá reprodukovatelnost chemické reakce
- derivatizační reakce musí probíhat rychle, reakce může probíhat za extrémních podmínek (pH, teplota)
- používá se nadbytek reakčního činidla a dochází tak ke zřeďování mobilní fáze činidlem a dochází ke snížení účinnosti separace vlivem rozmytí chromatografické zóny
- reakce může být neselektivní, vedlejší produkty reakce nejsou na závadu
- není nutné hledat nové podmínky separace, neboť se vzorek separuje v nezměněné podobě
- vysoké náklady na techniku, neboť se musí používat speciální zařízení a reaktory, v nichž je nutno provádět řadu operací, výhodou je automatizace procesu derivatizace
- veškeré manuální operace jsou eliminovány
1.1 Reaktory používané za chromatografickou kolonou
Derivatizace za kolonou se někdy rovněž nazývá on-line derivatizace a jedná se o průtočný reaktor, který je umístěn za chromatografickou kolonu. V průběhu reakce dochází k rozmývání zóny v celém systému, které je nutno potlačit na minimum,
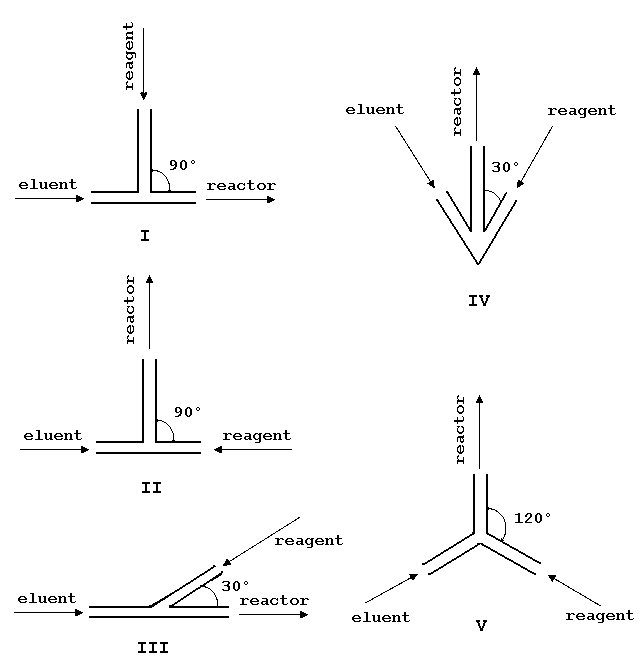
čehož se dosáhne vhodnou konstrukcí reaktoru, směšovačů (více také naleznete zde...) a spojovacího potrubí. Konstrukce (objem a tvar) směšovacích kusů má vliv na rozmytí eluční zóny, promísení eluentu a činidla a na šum detektoru. Různé konstrukce a řešení směšovacích kusů jsou ukázány na obrázku č. 1. Obecně se volí taková konstrukce, aby docházelo při mísení ke vzniku turbulentního toku a rozmytí eluční zóny přitom bylo co nejmenší. K tomuto účelu je nejvhodnější konstrukce uvedená na obrázku č. 1 pod čísly III a IV. Další účinné mixéry jsou cyklónový mixer a rotační průtočný mixer.
Obr. č. 1 Různé konstrukce směšovacích kusů
|
Rozeznáváme v podstatě tři druhy postkolonové derivatizace:
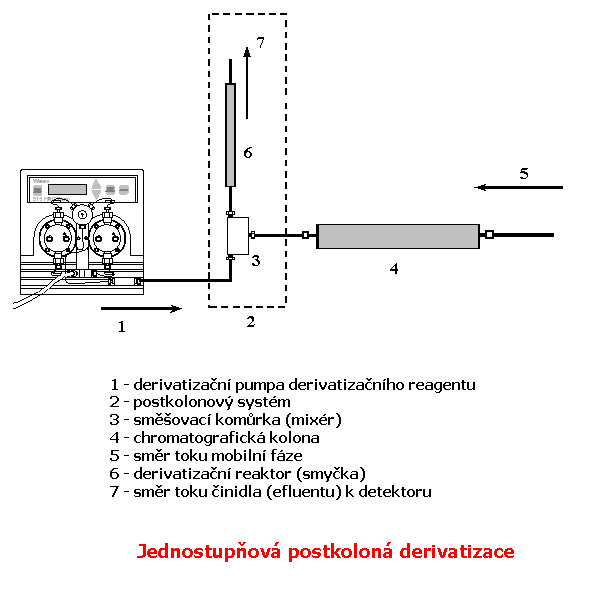
1.1.1 Jednostupňová derivatizace
V tomto případě reakce probíhá v jednom reakčním kroku
|
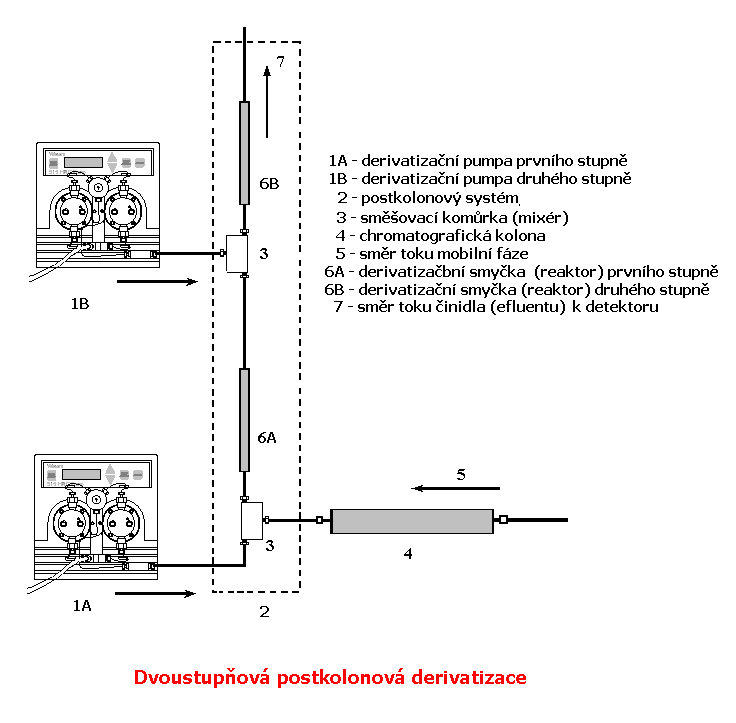
1.1.2 Dvoustupňová derivatizace
Reakce probíhá ve dvou reakčních krocích - např. v prvním kroku dochází k oxidaci analytu a následně k jeho reakci s derivatizačním činidlem
|
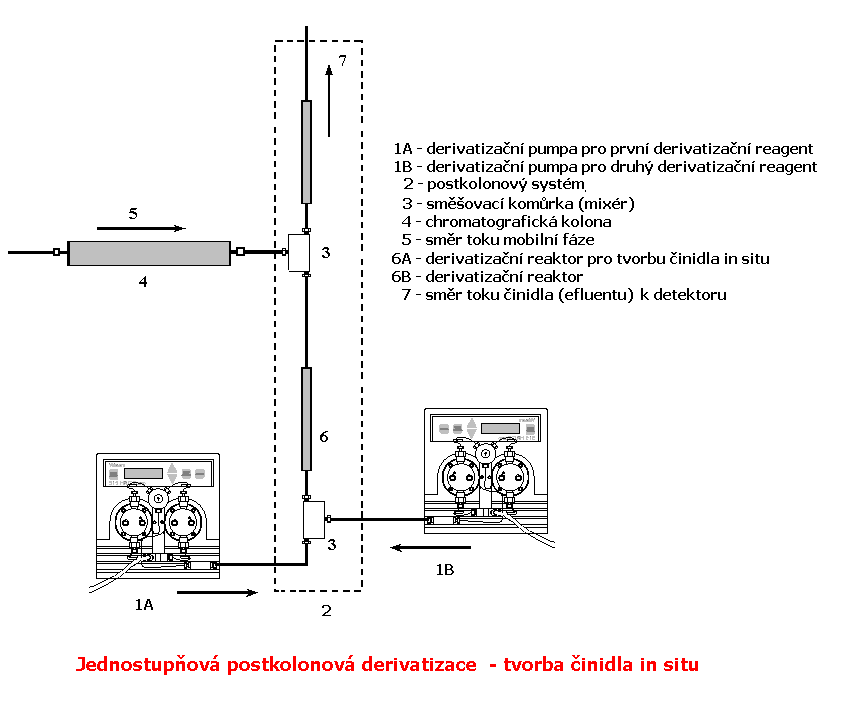
1.1.3 Jednotupňová derivatizace s tvorbou derivatizačního činidla in situ
Činidlo se tvoří v reaktoru mísením dvou různých činidel (např. z důvodu nízké stability vznikajícího činidla)
|
Obr. č. 2 Derivatizační jednotka - dvoustupňová derivatizace (firma Science Instruments and Software, s.r.o. ČR)

|
Výrobci postkolonových derivatizačních jednotek (zařízení):
Pickering Laboratories
Science Instruments and Software
ASI
Analytical Instruments, LLC
SENSIVATE, ChromTech
2. Derivatizační techniky v průtokových reaktorech
2.1 Teorie toku mobilní fáze postkolonovým reaktorem
V průběhu derivatizační reakce za kolonou dochází k rozmývání zóny v celém systému, které je nutno potlačit na minimum. Toho se dosáhne vhodnou konstrukcí reaktoru, směšovačů a spojovacího potrubí. Teorie toku mobilní fáze postkolonovým reaktorem.
2.2 Derivatizační techniky využívající tvorby derivátů reakcí s činidly v kapalné fázi
Tato technika je nejrozšířenější a je realizována v derivatizačním reaktoru, kdy do proudu mobilní fáze vycházející z kolony je aplikováno ve směšovací komůrce (zpravidla T-kusu, jejichž konstrukce je popsána řadou autorů [1],[2],[3] reakční médium, které vyvolá požadovanou reakci v samotném reaktoru, který může být termostatován.
Na tento typ derivatizace jsou kladeny určité požadavky:
kapalný reagent musí být mísitelný s mobilní fází
nesmí docházet k reakci činidla a mobilní fáze
musí vznikat struktury poskytující charakteristické absorpce v UV-VIS oblasti nebo vykazují fluorescenci
využívají se i reakce redoxní, hydrolytické nebo vyvolávající změnu pH
2.3 Reakce vyvolaná změnou pH před vstupem do detektoru
Do této skupiny derivatizačních technik jsou zařazeny reakce, kdy nevznikají nové deriváty,avšak změnou pH dojde k výrazné změně absorpce v oblasti UV nebo fluorescence.[4]
2.4 Derivatizační reakce v systému tuhá látka kapalina
Vlastní reakce probíhá na povrchu tuhé fáze, která může vystupovat jako vlastní reagent, katalysátor nebo nosič vázané látky (zpravidla enzymu). Výhodou této techniky je, že nedochází ke zřeďování mobilní fáze činidlem a vliv na rozšíření chromatografické zóny je minimální. Pěkný příklad postkolonové derivatizace v systému tuhá látka-kapalina je stanovení nízkých hladin vitaminu K s fluorimetrickou detekcí. Vitamin K je redukován na hydronaphtochinon po předchozí hydrolýze. K redukci vitaminu K se používají tři způsoby redukce - postkolonová derivatizace s kovovým zinkem,[5] redukce elektrochemická nebo fotochemická redukce. Vitamin K1 může být redukován na příslušný hydrochinon (K1H2 kovovým zinkem za přítomnosti iontů zinku: